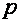 , удельный объём
, удельный объём 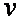 и абсолютная температура
и абсолютная температура 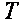 . Эти три параметра носят название термических параметров состояния.
. Эти три параметра носят название термических параметров состояния.
Исторически термодинамика возникла как наука, изучающая переход теплоты в механическую работу, что диктовалось необходимостью дать теоретические основы работы тепловых машин.
Принцип построения термодинамики довольно прост. В ее основу положены три экспериментальных закона и уравнение состояния: первый закон (первое начало термодинамики) — закон сохранения и превращения энергии; второй закон (второе начало термодинамики) указывает направление, по которому протекают естественные явления в природе; третий закон (третье начало термодинамики) утверждает, что абсолютный нуль температуры недостижим.
Термодинамическая система — тело (совокупность тел), способное (способных) обмениваться с другими телами (между собой) энергией и веществом.
Термодинамическая система имеет границы, отделяющие ее от окружающей среды. Границы термодинамической системы могут быть как реальными (газ в резервуаре, граница раздела фаз), так и чисто условными в виде контрольной поверхности.
Термодинамическая система может энергетически взаимодействовать с окружающей средой и с другими системами, а также обмениваться с ними веществом. В зависимости от условий взаимодействия с другими системами различают изолированную, замкнутую, открытую и адиабатно изолированную термодинамические системы.
Термодинамическая система, которая не может обмениваться энергией и веществом с другими системами, называется изолированной. В такой системе отдельные части (подсистемы) могут взаимодействовать между собой. Термодинамическая система называется закрытой, если она не может обмениваться веществом с другими системами. Термодинамические системы, которые могут обмениваться веществом с другими системами, называются открытыми.
Термодинамическая система, которая не может обмениваться теплотой с другими системами (окружающей средой), называется теплоизолированной или адиабатно изолированной.
С окружающей средой термодинамическая система может энергетически взаимодействовать посредством передачи теплоты и производства работы.
По роли отдельных тел, входящих в термодинамическую систему, их делят на рабочие тела (РТ), источники теплоты (ИТ) и объекты работы (ОР).
Рабочими телами являются, как правило, газообразные вещества - газы и пары, которые способны значительно изменять свой объём при изменении внешних условий.
В тех состояниях, когда можно пренебречь влиянием сил взаимодействия между молекулами и объёмом самих молекул (сильно нагретый газ при небольших давлениях), газ называют идеальным. В противном случае газ называется реальным.
Рабочее тело в тепловой машине получает или отдаёт теплоту, взаимодействуя с более нагретыми или более холодными внешними телами. Такие тела носят название источников теплоты.
Тело, которое отдаёт теплоту рабочему телу и не изменяет свою температуру, называется верхним источником теплоты (ВИТ) или теплоотдатчиком. Тело, которое получает теплоту от рабочего тела и не изменяет свою температуру, называется нижним источником теплоты (НИТ) или теплоприёмником.
Совокупность физических свойств системы в рассматриваемых условиях называют термодинамическим состоянием системы.
Различают равновесное (стационарное) и неравновесное (нестационарное) состояния термодинамической системы.
Макроскопические величины (т. е. величины, которые характеризуют тело в целом), характеризующие физические свойства тела в данный момент, называются термодинамическими параметрами состояния. Последние разделяются на интенсивные (не зависящие от массы тела) и на экстенсивные (пропорциональные массе тела).
К основным параметрам состояния, поддающимся непосредственному измерению простыми техническими средствами, относятся абсолютное давление 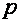 , удельный объём
, удельный объём 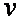 и абсолютная температура
и абсолютная температура 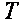 . Эти три параметра носят название термических параметров состояния.
. Эти три параметра носят название термических параметров состояния.
К параметрам состояния относятся также внутренняя энергия 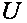 , энтальпия
, энтальпия 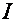 и энтропия
и энтропия 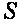 , которые носят название калорических параметров состояния.
, которые носят название калорических параметров состояния.
Равновесным состоянием термодинамической системы называется такое состояние, которое характеризуется при постоянных внешних условиях неизменностью параметров во времени и отсутствием в системе потоков. Состояние термодинамической системы, при котором во всех ее частях температура одинакова, называют термическим равновесным состоянием.
Изолированная термодинамическая система независимо от своего начального состояния с течением времени всегда приходит в состояние равновесия. Необходимо отметить, что никогда самопроизвольно выйти из него система не может (основной постулат термодинамики — нулевое начало).
Состояние термодинамической системы, при котором значения параметров во всех частях ее остаются неизменными во времени благодаря внешнему воздействию потоков вещества, энергии, импульса, заряда и т. п., называется стационарным. Если значения параметров изменяются во времени, то состояние термодинамической системы называется нестационарным.
Любое изменение в термодинамической системе, связанное с изменением хотя бы одного из ее параметров, называется термодинамическим процессом. Если одна система совершает работу над другой системой с помощью механических и электрических сил, то взаимодействие называется механическим. Взаимодействие, которое приводит к изменению энергии и совершается в форме передачи теплоты посредством теплопроводности или тепловой радиации, называется тепловым. Взаимодействие, приводящее к изменению энергии и совершаемое в форме передачи массы, называется массообменным.
Различают равновесные и неравновесные процессы.
Равновесным процессом называется термодинамический процесс, представляющий собой непрерывную последовательность равновесных состояний. В таком процессе физические параметры изменяются бесконечно медленно, так что система все время находится в равновесном состоянии. Кроме того, все части системы имеют одинаковые температуру и давление.
Неравновесным процессом называется термодинамический процесс, представляющий собой последовательность состояний, среди которых не все являются равновесными. В неравновесном процессе различные части системы имеют разные температуры, давления, плотности, концентрации.
Если термодинамическая система выведена из состояния равновесия и предоставлена сама себе, то через некоторый промежуток времени она снова придет в состояние равновесия. Процесс перехода системы из неравновесного состояния в равновесное называется релаксацией, а время перехода в состояние равновесия — временем релаксации.
К термическим параметрам состояния относятся давление 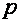 , объем
, объем 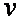 , температура
, температура 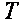 .
.
К калорическим параметрам состояния относятся следующие основные термодинамические величины: энтропия 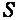 , внутренняя энергия
, внутренняя энергия 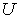 и энтальпия
и энтальпия 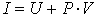 .
.
Давление — физическая величина, численно равная отношению нормальной составляющей силы к площади, на которую действует эта сила.
Единицей давления в СИ является паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью 1 м2 (1Па=1 Н/м2). Часто приходится измерять давление высотой столба какой-либо жидкости (воды, ртути и др.).
В табл. 1.1 приведены соотношения между ранее применявшимися единицами измерения давления и единицами давления в СИ.
Таблица 1.1 |
||||||
Единица |
Па |
бар |
кгс/см2 |
мм рт.ст. |
мм вод.ст. |
|
1 Па |
1 |
10-5 |
1,02·10-5 |
7,5024·10-3 |
1,02·10-1 |
|
1 бар |
105 |
1 |
1,02 |
7,5024·102 |
1,02·104 |
|
1 кгс/см2 |
9,8067·104 |
0,98067 |
1 |
735 |
104 |
|
1 мм рт.ст. |
133 |
1,33·10-3 |
1,36·10-3 |
1 |
13,6 |
|
| 1 мм вод.ст. |
9,8067 |
9,8067·10-5 |
10-4 |
7,35·10-2 |
1 |
|
Различают атмосферное, или барометрическое, давление 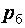 , абсолютное давление
, абсолютное давление 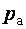 , манометрическое, или избыточное, разрежение, или вакуум.
, манометрическое, или избыточное, разрежение, или вакуум.
Давление, создаваемое атмосферным воздухом, называется барометрическим, или атмосферным.
Абсолютным давлением 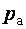 называется давление, отсчитываемое от нуля (абсолютного вакуума).
называется давление, отсчитываемое от нуля (абсолютного вакуума).
Избыточным, или манометрическим, давлением называется давление сверх атмосферного, то есть избыточное давление — это разность между абсолютным и барометрическим давлениями: 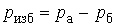 .
.
Разрежением, или вакуумом, называется разность между атмосферным давлением и абсолютным давлением той среды, где измеряется давление. Если абсолютное давление газа или пара в сосуде ниже барометрического, то есть 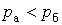 , то разность
, то разность 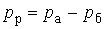 называется разрежением, или вакуумом.
называется разрежением, или вакуумом.
Вакуум показывает, насколько давление газа (пара) меньше давления окружающей среды. Давление атмосферного воздуха измеряется барометрами, избыточное давление — манометрами, а давление разрежения — вакуумметрами.
В термодинамических уравнениях всегда используют значения абсолютного давления ввиду того, что оно является параметром, характеризующим состояние термодинамической системы.
Атмосферное давление — величина переменная, поэтому в технике применяется нормальное атмосферное давление, 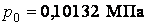 (760 мм рт. ст.).
(760 мм рт. ст.).
Температура тела есть мера его нагретости. Температура определяет направление передачи теплоты. Если два тела А и В имеют соответственно температуру Т1 и Т2 и Т1>Т2, то теплота переходит от тела А к телу В. При этом температура тела А уменьшается, а тела В - увеличивается.
С точки зрения молекулярно-кинетической теории температура есть мера интенсивности теплового движения молекул.
В термодинамике рассматривают температуру как среднестатистическую величину, которая характеризует систему, состоящую из очень большого числа молекул (частиц), находящихся в хаотическом (тепловом) движении. Поэтому к единичным молекулам понятие температуры не применимо. При температуре абсолютного нуля тепловое движение молекул отсутствует. Эта предельная минимальная температура называется абсолютным нулем и является началом для отсчета температур. Понятно, что не может быть 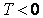 , то есть абсолютная температура всегда положительна.
, то есть абсолютная температура всегда положительна.
Температура, отсчитываемая от абсолютного нуля, называется абсолютной, а шкала температур называется шкалой Кельвина.
Практически измерять кинетическую энергию молекул газа непосредственно невозможно. Поэтому для измерения температуры используют различные косвенные методы. Температура измеряется при помощи различных термодинамических устройств - термометров).
Использование термометров основано на том факте, что два соприкасающихся тела с разными температурами через некоторое время приходят к состоянию теплового равновесия и принимают одинаковую температуру.
Численный отсчет температуры производится по шкале температур. За основную единицу измерения температуры принимают градус, имеющий разную величину в различных температурных шкалах. Шкала температур устанавливается путем деления разности показаний термометра в двух произвольно выбранных постоянных температурных точках, называемых реперными или опорными, на некоторое число равных частей — градусов.
Ввиду того, что выбор постоянных температурных точек и цены деления шкалы является произвольным, имеется ряд различных шкал температуры.
В настоящее время применяются различные температурные шкалы: Цельсия, Фаренгейта, Реомюра, Ранкина.
По шкале Цельсия (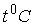 ) приняты следующие постоянные температурные точки: О°C — температура таяния льда, 100°C — температура кипения воды при нормальном атмосферном давлении.
) приняты следующие постоянные температурные точки: О°C — температура таяния льда, 100°C — температура кипения воды при нормальном атмосферном давлении.
В 1724 г. Фаренгейт предложил термометр, в качестве реперных точек которого приняты: +212°F — температура кипения воды при нормальном атмосферном давлении; +32°F - температура таяния льда. Разность температур кипения воды и таяния льда по шкале Фаренгейта равна 212°— 32° = 180 °F, а по шкале Цельсия — 100°C. Следовательно, 1°F соответствует 5/9 °C, а 1°C — 1,8°F.
Шкала Реомюра (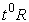 ) имеет следующие реперные точки: О°R — температура таяния льда, 80°R — температура кипения воды при нормальном атмосферном давлении.
) имеет следующие реперные точки: О°R — температура таяния льда, 80°R — температура кипения воды при нормальном атмосферном давлении.
Шкала Ранкина (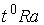 ) — это шкала Фаренгейта, отсчитанная от абсолютного нуля. В этой шкале температура таяния льда
) — это шкала Фаренгейта, отсчитанная от абсолютного нуля. В этой шкале температура таяния льда 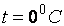 (T0=273,15 К) соответствует 491,67°Ra, а температура кипения воды при нормальном атмосферном давлении (T0=373,15 К) соответствует 671,67°Ra.
(T0=273,15 К) соответствует 491,67°Ra, а температура кипения воды при нормальном атмосферном давлении (T0=373,15 К) соответствует 671,67°Ra.
Решением Международного комитета мер и весов приняты две шкалы: термодинамическая температурная шкала, которая принята основной, и Международная практическая температурная шкала (МПТШ-68), выбранная таким образом, чтобы температура, измеренная по этой шкале, была близка к термодинамической. В основу построения термодинамической шкалы положен тот факт, что в циклах Карно, располагающихся между двумя адиабатами, разность температур изотерм считается постоянной, если в механическую работу превращаются одинаковые количества теплоты. Наиболее универсальной шкалой температур является абсолютная термодинамическая шкала температур — шкала Кельвина.
В шкале Кельвина используется единственная экспериментальная реперная точка — тройная точка химически чистой воды (в термодинамическом равновесии находятся три агрегатных состояния; лед, жидкая вода и пар). Этому состоянию соответствует температура 273,15К (0,01°С). Второй постоянной точкой является абсолютный нуль температур (0К). Кельвин — единица измерения температуры по термодинамической температурной шкале, равная 1/273,15 части интервала от абсолютного нуля температуры до температуры тройной точки воды.
Практическим осуществлением термодинамической шкалы температур является Международная практическая температурная шкала. В этой шкале используется одиннадцать реперных точек. В табл. 1.2 приведены значения основных реперных точек.
Таблица 1.2 |
||
Равновесное состояние |
МПШТ-68 |
|
T68 |
t68 |
|
Точка кипения кислорода |
90,188 К |
-182,962 0C |
Тройная точка воды |
273,16 К |
+0,01 0C |
Точка кипения воды |
373,15 К |
+100,0 0C |
| Точка плавления цинка |
692,73 К |
+419,58 0C |
| Точка плавления серебра |
1235,08 К |
+961,93 0C |
| Точка плавления золота
|
1337,58 К |
+1064,43 0C |
| Температуры кипения и плавления даны при давлении 101325 Па |
||
Удельный объем вещества — это объем, занимаемый единицей массы данного вещества.
Плотность вещества 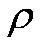 — величина, обратная удельному объему и определяющая количество вещества, заключенное в единице объема.
— величина, обратная удельному объему и определяющая количество вещества, заключенное в единице объема.
Единица плотности в СИ — кг/м3, в системе СГС — г/см3. Плотность и удельный объем зависят от температуры и давления, то есть от термодинамического состояния вещества. Обычно в справочниках приводятся их значения при нормальных физических условиях. За нормальные физические условия принимают давление, равное 101,325 кПа (760 мм рт. ст.), и температуру, равную О °С.
Количество вещества. Единицей количества вещества в СИ является моль. Кроме моля применяют кратные и дольные части от моля (кмоль, Ммоль и др.). Количество вещества — это физическая величина, определяемая числом структурных элементов (атомов, молекул, ионов, электронов). Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг.
Молярной массой вещества называют отношение массы вещества к его количеству:
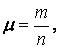
|
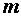 выразить в кг,
выразить в кг, 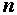 — в молях, μ — выразится в кг/моль.
— в молях, μ — выразится в кг/моль.
К калорическим параметрам состояния относятся, как уже отмечалось, внутренняя энергия 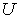 , энтальпия
, энтальпия 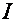 и энтропия
и энтропия 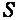 . Своим названием эти параметры обязаны тому, что ранее измерялись в калориях.
. Своим названием эти параметры обязаны тому, что ранее измерялись в калориях.
Внутренняя энергия. Любая термодинамическая система в каждом состоянии обладает запасом полной энергии 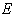 , которая состоит из внутренней энергии
, которая состоит из внутренней энергии 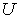 , зависящей от внутреннего состояния тела, и внешней энергии
, зависящей от внутреннего состояния тела, и внешней энергии 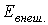 , связанной с движением тела как целого и положением его в каком-либо внешнем поле сил (например в поле сил тяжести), т. е.
, связанной с движением тела как целого и положением его в каком-либо внешнем поле сил (например в поле сил тяжести), т. е.
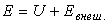
|
Если тело не движется, а влиянием внешнего поля сил можно пренебречь, то полная энергия будет представлять собой только внутреннюю энергию.
Любая термодинамическая система (рабочее тело) обладает запасом внутренней энергии, которая состоит из энергии хаотического (теплового) движения и взаимодействия молекул. Поскольку внутренняя энергия рабочего тела зависит от его массы, обычно интересуются значением внутренней энергии, отнесенной к 1 кг массы тела, — удельной внутренней энергией
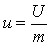 . .
|
В общем случае удельная кинетическая энергия теплового движения состоит из удельной кинетической энергии поступательного, вращательного и колебательного движений молекул, зависящей только от температуры рабочего тела, и удельной потенциальной энергии взаимодействия молекул между собой, которая, в свою очередь, зависит от среднего расстояния между молекулами, т. е. от занимаемого рабочим телом объёма. Следовательно, в общем случае удельная внутренняя энергия рабочего тела зависит от его температуры 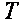 и удельного объема
и удельного объема 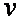 , являясь однозначной функцией этих параметров состояния:
, являясь однозначной функцией этих параметров состояния: 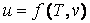 , или
, или
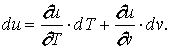 . .
|
Таким образом, важнейшим свойством удельной внутренней энергии рабочего тела является то, что она представляет собой однозначную функцию состояния тела, определяемого любой парой его основных параметров ( 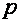 ,
, 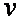 ,
, 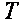 ), и сама может служить параметром состояния. Из этого свойства следует, что изменение удельной внутренней энергии не зависит от характера процесса, а определяется лишь начальным и конечным состояниями рабочего тела. Следовательно, бесконечно малое приращение удельной внутренней энергии является полным дифференциалом
), и сама может служить параметром состояния. Из этого свойства следует, что изменение удельной внутренней энергии не зависит от характера процесса, а определяется лишь начальным и конечным состояниями рабочего тела. Следовательно, бесконечно малое приращение удельной внутренней энергии является полным дифференциалом 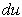 .
.
В идеальном газе силы взаимодействия между молекулами отсутствуют и удельная потенциальная энергия его равна нулю. Поэтому удельная внутренняя энергия идеального газа состоит только из удельной кинетической энергии движения молекул 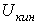 и определяется его температурой:
и определяется его температурой: 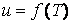 , или
, или

|
В замкнутом (круговом) процессе, в котором начальное и конечное состояния совпадают, изменение удельной внутренней энергии равно нулю.
Определять абсолютное значение удельной внутренней энергии в большинстве технических расчетов не требуется, так как обычно необходимо знать только ее изменение. Поэтому условно приписывают некоторому состоянию рабочего тела нулевое значение удельной внутренней энергии, а все расчеты ведут относительно этого значения.
Энтальпия. Рассмотрим полную энергию газа, находящегося под давлением 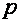 , создаваемым грузом массой
, создаваемым грузом массой 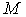 (рис. 1.1). В этом случае полная энергия
(рис. 1.1). В этом случае полная энергия 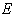 системы состоит из внутренней энергии газа
системы состоит из внутренней энергии газа 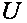 и потенциальной энергии груза, равной
и потенциальной энергии груза, равной 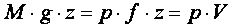 , где
, где 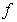 - площадь поперечного сечения поршня. Т. е.
- площадь поперечного сечения поршня. Т. е. 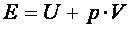 . Величина
. Величина 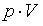 , зависящая от сил, действующих на поршень, получила название потенциальной энергии давления.
, зависящая от сил, действующих на поршень, получила название потенциальной энергии давления.

|
|
Рис. 1.1. К определению энтальпии газа
|
Таким образом, если газ находится в среде с давлением 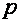 , то с любым состоянием его связана некоторая энергия
, то с любым состоянием его связана некоторая энергия 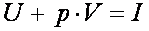 , получившая название энтальпии газа в данном состоянии. Выражение энтальпии для 1 кг газа (т. е. удельной энтальпии) имеет вид
, получившая название энтальпии газа в данном состоянии. Выражение энтальпии для 1 кг газа (т. е. удельной энтальпии) имеет вид
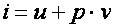 . .
|
Следовательно, удельная энтальпия, будучи зависимой от параметров состояния 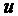 ,
, 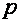 и
и 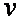 , также является параметром состояния. Поэтому изменение
, также является параметром состояния. Поэтому изменение 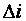 , как и изменение
, как и изменение 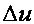 , не зависит от характера процесса, а определяется только начальным и конечным состояниями, т. е.
, не зависит от характера процесса, а определяется только начальным и конечным состояниями, т. е.
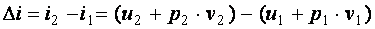 . .
|
Как однозначная функция состояния удельная энтальпия может быть представлена в виде функции любой пары основных параметров состояния.
Удельная энтальпия идеального газа, как и его удельная внутренняя энергия, является функцией только температуры. Действительно:
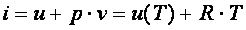 . .
|
Удельная энтальпия, как и удельная внутренняя энергия, выражается в джоулях на килограмм (Дж/кг).
Энтропия. Кроме рассмотренных параметров, в термодинамике широко используется еще один калорический параметр состояния — энтропия 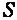 , введенный Клаузиусом в 1865 г. при анализе круговых процессов.
, введенный Клаузиусом в 1865 г. при анализе круговых процессов.
Энтропия — параметр состояния, дифференциал которого равен отношению бесконечно малого количества теплоты 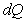 в элементарном обратимом процессе к абсолютной температуре
в элементарном обратимом процессе к абсолютной температуре 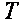 , постоянной на бесконечно малом участке процесса, т.е.
, постоянной на бесконечно малом участке процесса, т.е.
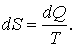
|
Если количество теплоты отнести к 1 кг вещества (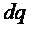 ), то получим удельную энтропию
), то получим удельную энтропию
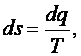
|
Бойль в 1662 году и Мариот в 1676 году обнаружили, что при 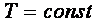
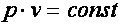 .
.
Гей-Люссак в 1802 году опытным путём установил, что при 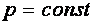
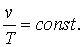
В 1811 году Авогадро выдвинул гипотезу: одинаковые объёмы различных газов при одинаковых физических условиях содержат одинаковые количества молекул. Эта гипотеза, став после её доказательства законом, приводит к одному важному следствию, согласно которому при одинаковых физических условиях для любых газов произведение молекулярной массы газа на его удельный объём есть величина постоянная, т. е. 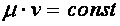 .
.
Напомним, что молекулярной массой называется количество вещества в граммах, численно равное его молекулярной массе. Например, молекулярная масса углерода равна 12 граммам, а кислорода - 32 граммам.
Произведение 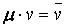 представляет собой объём одного моля газа, который при нормальных физических условиях равен 22,4 м3.
представляет собой объём одного моля газа, который при нормальных физических условиях равен 22,4 м3.
Отметим, что нормальным физическим условиям соответствуют 760 мм рт. ст. и 00С, а нормальным техническим условиям - 735 мм рт. ст. и 100С.
Сопоставление законов Бойля-Мариота и Гей-Люссака приводят к обобщённому закону Бойля-Гей-Люссака:
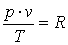 , ,
|
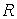 - характеристическая постоянная идеального газа (при нормальных физических условиях
- характеристическая постоянная идеального газа (при нормальных физических условиях 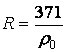
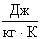 , где
, где 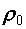 - плотность при нормальных физических условиях).
- плотность при нормальных физических условиях).
Это уравнение, полученное Клайпероном в 1834 году, называется уравнением состояния идеальных газов или уравнением Клайперона.
Выше отмечалось, что любое изменение состояния рабочего тела, которое происходит в результате его энергетического взаимодействия с окружающей средой, представляет собой термодинамический процесс. В общем случае энергообмен в термодинамическом процессе может осуществляться посредством работы L либо теплоты Q. Работа и теплота являются энергетическими характеристиками термодинамического процесса.
Механическая работа против внешних сил, связанная с изменением объема, определяется выражением
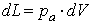 , ,
|
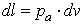 , ,
|
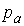 — абсолютное давление (потенциал механического взаимодействия),
— абсолютное давление (потенциал механического взаимодействия), 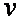 — удельный объем (координата механического взаимодействия).
— удельный объем (координата механического взаимодействия).
Для конечного процесса, при котором объем изменяется от 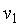 до
до 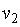 , общее выражение удельной термодинамической работы следует записать так:
, общее выражение удельной термодинамической работы следует записать так:
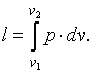
|
|
|
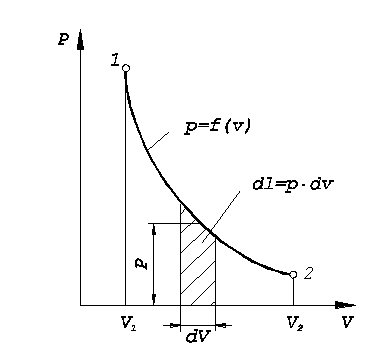
Рис. 1.2. К вычислению работы в термодинамическом процессе
|
В общем случае давление 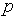 — величина переменная, зависящая от
— величина переменная, зависящая от 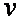 . Для определения интеграла должна быть известна зависимость между
. Для определения интеграла должна быть известна зависимость между 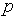 и
и 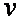 в данном процессе, т. е. надо знать уравнение процесса
в данном процессе, т. е. надо знать уравнение процесса 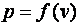 . Графически эта зависимость может быть изображена в
. Графически эта зависимость может быть изображена в 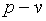 -координатах кривой 1-2 (рис. 1.2).
-координатах кривой 1-2 (рис. 1.2).
Очевидно, численно удельная работа будет зависеть от характера кривой процесса и изображается в 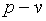 -координатах площадью, ограниченной кривой процесса, двумя ординатами и осью абсцисс.
-координатах площадью, ограниченной кривой процесса, двумя ординатами и осью абсцисс.
При вычислении интеграла обнаруживается, что если объём рабочего тела уменьшается, то величина интеграла отрицательна, и наоборот. Поэтому если рабочему телу сообщается потенциальная энергия путём его сжатия, то работа изменения объёма есть величина отрицательная. Если же рабочее тело совершает работу расширяясь, то работа изменения объёма - положительна.